
Evaluación in vitro y acoplamiento molecular de QS-21 y ácido quiláico de Quillaja saponaria Molina como agentes contra el cáncer gástrico
Resumen
Se estudió el mecanismo citotóxico de la saponina QS-21 y su aglicona ácido quiláico (QA) en células de cáncer gástrico humano (SNU1 y KATO III). Ambos compuestos mostraron actividad citotóxica in vitro con valores de IC50 7,1 μM (QS-21) y 13,6 μM (QA) en células SNU1; 7,4 μM (QS-21) y 67 μM (QA) en células KATO III. QS-21 y QA inducen la apoptosis en SNU1 y KATO III, como demuestran los ensayos TUNEL, Annexin-V y Caspasa. Además, realizamos estudios de acoplamiento in silico simulando la unión de ambos compuestos triterpénicos a proteínas clave implicadas en las vías apoptóticas. Las energías de unión (∆Gbin) así calculadas, sugieren que la proteína proapoptótica Bid podría ser una diana plausible implicada en el efecto apoptótico de ambos compuestos triterpénicos. Aunque el QA muestra algunos efectos antiproliferativos en las células SNU1 cultivadas in vitro, nuestros resultados sugieren que el QS-21 es un agente antitumoral más potente, lo que merece una investigación más profunda en relación con sus propiedades como posibles agentes terapéuticos para el cáncer gástrico.
Introducción
El cáncer gástrico (CG) es la tercera neoplasia tumoral más mortífera en todo el mundo. A pesar de un descenso general de la incidencia en las últimas décadas, el CG sigue siendo el quinto tipo de cáncer más frecuente1. Por desgracia, la multirresistencia a los fármacos ha afectado negativamente a la eficacia de muchas formas de quimioterapia2. Una forma de aumentar la eficacia de la quimioterapia es la combinación sinérgica de los fármacos anticancerosos tradicionales con compuestos vegetales (fitoquímicos)3; un enfoque aún más prometedor es el uso de fitoquímicos como agentes antitumorales en lugar de los fármacos anticancerosos tradicionales, para reducir los efectos adversos relacionados con esos fármacos: toxicidad en los tejidos normales y resistencia a los fármacos. Un grupo notable de fitoquímicos son las saponinas, una familia muy extendida de glucósidos naturales de agliconas esteroides o triterpenoides4. La corteza de Quillaja saponaria Molina (QS) -un árbol de hoja perenne originario de Chile- se utiliza ampliamente como fuente de saponinas fisiológicamente activas basadas en la aglicona triterpénica ácido quilláico (QA). Este último es un triterpenoide pentacíclico, es decir, olean-12-eno sustituido por grupos hidroxi en las posiciones 3 y 16, un grupo oxo en la posición 23 y un grupo carboxilo en la posición 28. Las saponinas de Q. saponaria tienen una estructura muy diversa; un miembro destacado de esa familia de compuestos es QS-216. El QS-21 es un glucósido triterpénico 3,28-bidesmódico acilado de la aglicona QA, como se muestra en la Fig. 1. La QA presenta diversas actividades biológicas, como hemolítica, antiinflamatoria, inmunoestimuladora, antinociceptiva, antivírica y citotóxica4,5,6. La mayoría de los estudios sobre los efectos biológicos de la QS-21 se han centrado en la respuesta inmunitaria; sin embargo, aún no se han estudiado los efectos citotóxicos y antiproliferativos tanto de la QS-21 como de la QA en líneas celulares humanas de GC6,7. Por otra parte, Wang et al.7 demostraron la actividad antitumoral in vitro de la QS-21 en 11 líneas celulares tumorales como melanoma, cáncer de mama, cáncer de pulmón de células pequeñas, cáncer de próstata.
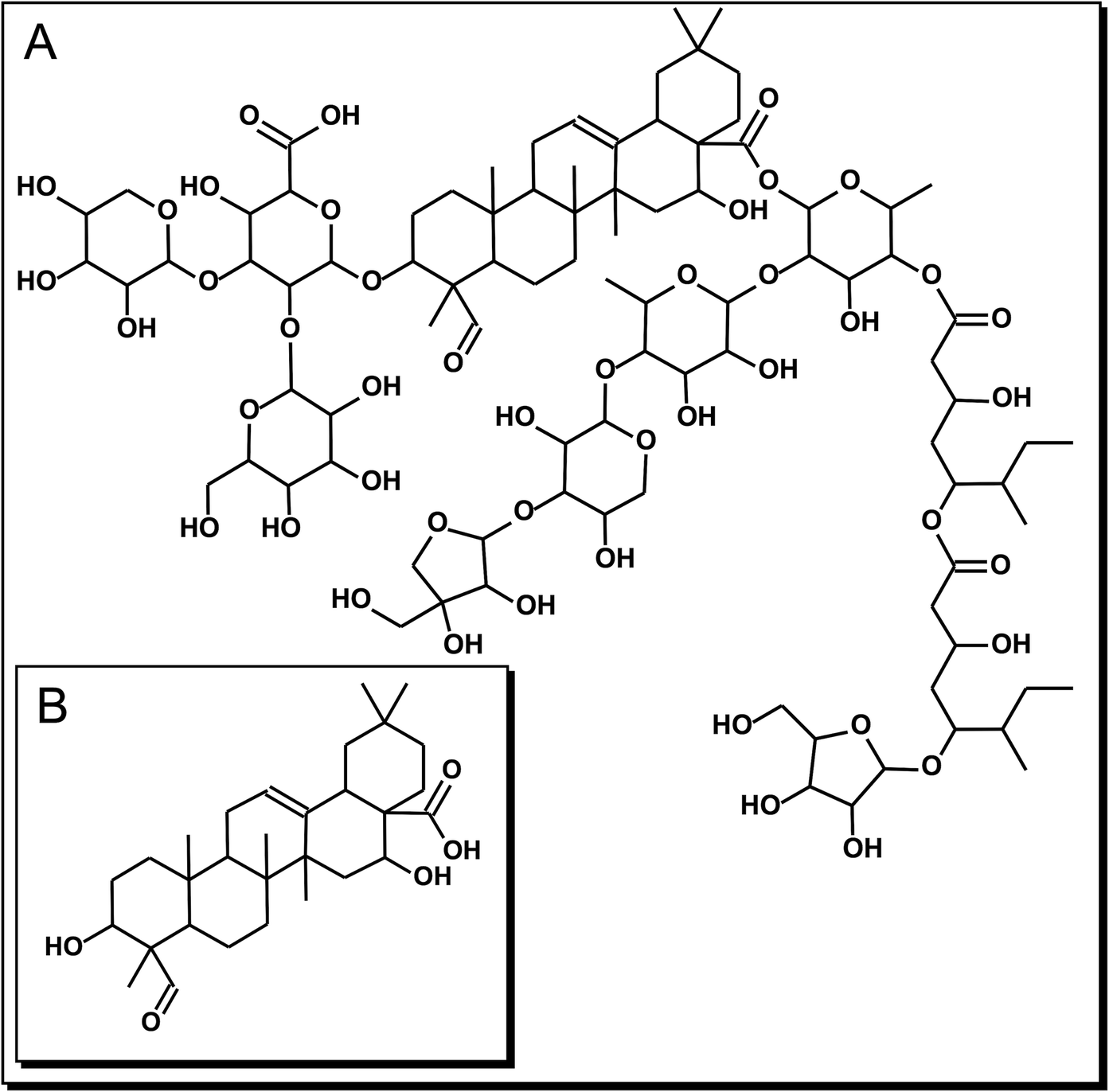
Figura 1. Estructura química de los compuestos triterpénicos empleados en este estudio. (A): QS-21: C92H148O46 y (B) QA: C30H46O5.
El objetivo de este estudio era determinar el potencial terapéutico in vitro y el mecanismo citotóxico de la saponina QS-21 y su aglicona QA en dos líneas celulares de GC humano (SNU1 y KATO III). Para complementar el estudio in vitro y obtener información sobre el mecanismo de acción de QS-21 y QA para desencadenar la muerte celular, realizamos estudios de acoplamiento molecular de estos compuestos con estructuras 3D conocidas de las proteínas implicadas en la señalización de la muerte celular, como el receptor de la muerte (DR4), la proteína FAS y la cinasa C-Jun-N-terminal (JNK1), la proteína cinasa RAC-alfa serina/treonina (AKT1), la proteína proapoptótica BAX, la BID y el receptor 2 del factor de crecimiento de fibroblastos (FGFR-2); Todas estas proteínas son componentes clave de la vía apoptótica extrínseca y están sobreexpresadas en las células de los tumores sólidos8,9,10.
Resultados
Ensayo de citotoxicidad de QS-21 y QA en células de cáncer gástrico (ensayos MTS y LDH)
Para determinar el potencial terapéutico de QS-21 y QA en el tratamiento del cáncer gástrico, comprobamos primero su impacto en la viabilidad de las líneas celulares in vitro KATO III, SNU1 y GES-1, mediante el ensayo MTS11.
Todos los tipos celulares en estudio se trataron con QS-21 y QA en diferentes rangos de concentración, durante 24 h y estaurosporina (STS) (véanse Material y métodos y Fig. suplementaria S1). QA y QS-21 fueron citotóxicos para las líneas tumorales KATO III y SNU1 de forma dependiente de la dosis (Fig. 2A, B); ambos compuestos apenas fueron citotóxicos para las células GES-1, una línea celular humana normal empleada como control (Fig. 2A, B). QA mostró una actividad citotóxica, que fue más pronunciada en las células SNU1 que en las KATO III -valor IC50 de 13,6 µM y 67 µM, respectivamente (Fig. 2B, Tabla 1). También hay que señalar que SNU1 fue más sensible a concentraciones superiores a 16,0 µM de QA. En las condiciones ensayadas, QS-21 mostró un efecto citotóxico mayor que QA en las dos líneas celulares cancerosas estudiadas, con valores IC50 de 7,1 μM y 7,4 μM respectivamente.
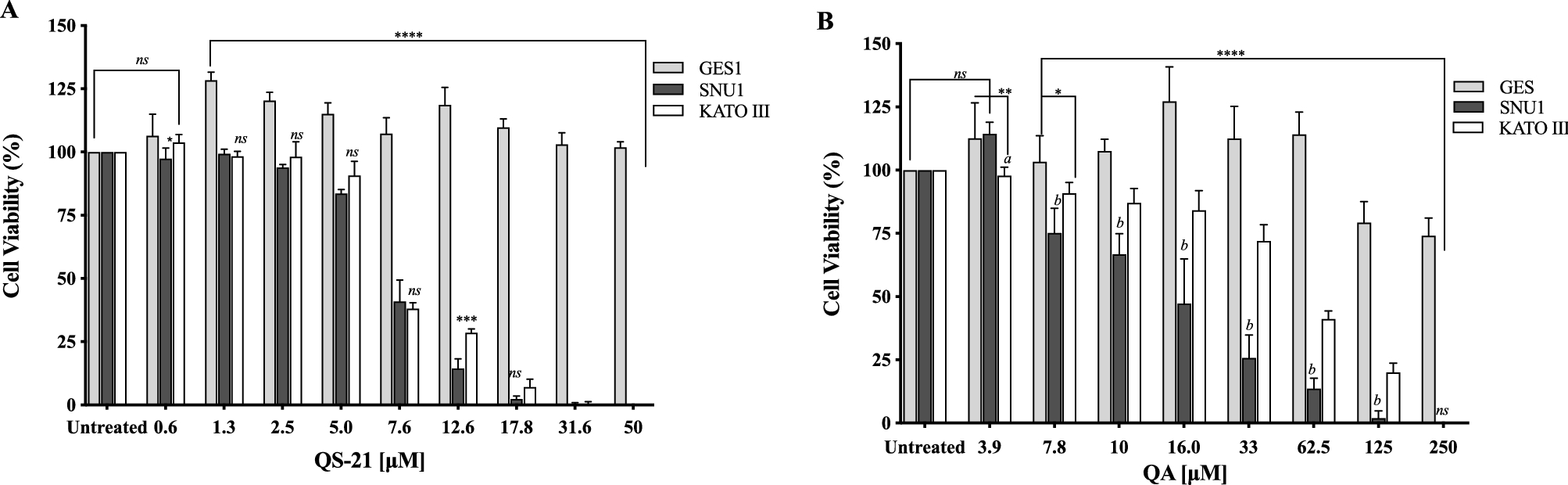
Figura 2. Efecto de QS-21 y QA sobre la viabilidad celular mediante el ensayo MTS. Los datos se expresan como media ± DE de cinco experimentos independientes. (A) ****P<0,0001 cuando SNU1 y KATO III se compararon con GES-1, ***P<0,005 SNU1 frente a KATO III, *P<0,05 GES-1 frente a SNU1 y ns (no significativo) entre los grupos tratados. (B) ****P<0,0001 al comparar SNU1 y KATO III con GES-1, ** y *indican P<0,01 y P<0,05 GES-1 frente a KATO III, P<0,005 (a y b) KATO III frente a SNU1.
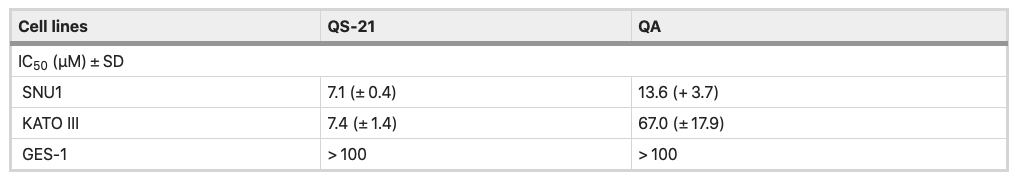
Tabla 1. Valores IC50 de QS-21 y QA en líneas celulares de cáncer gástrico y líneas celulares normales humanas gástricas.
QS-21 y QA son moléculas tensioactivas y, en las condiciones empleadas en los ensayos in vitro, ambos compuestos pueden interactuar con los componentes lipídicos de las membranas biológicas dando lugar a la formación de poros o incluso induciendo la ruptura parcial o total de las membranas. Además, algunas moléculas pueden generar la alteración de la integridad de las balsas lipídicas, dando lugar a una señal apoptótica o proapoptótica como la metil-β-ciclodextrina o la Avicina D12,13. Para determinar si la pérdida de viabilidad celular detectada por el método MTS en las células SNU1 y KATO III tras la exposición a QS-21 y QA era sólo consecuencia de la alteración de la membrana plasmática, o estaba implicado un mecanismo diferente, medimos la liberación de la enzima citosólica de la lactato deshidrogenasa (LDH) al medio extracelular tras la exposición de las células a ambos compuestos triterpénicos. Para ello, las células se expusieron a diferentes concentraciones de QS-21 y QA que oscilaban entre 0 y 1 × 103 µM. Aunque ambos compuestos tuvieron un efecto lítico sobre las células SNU1 y KATO III en el intervalo de concentración alto (Fig. 3), su impacto no fue significativo en el intervalo de concentraciones más bajo, en el que la prueba MTS reveló la pérdida de viabilidad celular, como se muestra en la Fig. 4. Por ejemplo, el valor de viabilidad estimado en términos de integridad de la membrana (determinado por la liberación de LDH) en las células SNU1 expuestas a las dosis IC50 para la alteración metabólica, para QA y QS-21 fueron del 78% y 72%, respectivamente, mientras que para las células KATO III fueron del 78% y 77%, respectivamente (Fig. 4). La liberación de cantidades significativas de LDH sólo se observó a concentraciones más altas de QA y QS-21 tanto en SNU1 como en KATO III (>100 µM), como se muestra en las Figs. 3A, B y 4. Este resultado demostró que QS-21 y QA tenían un efecto mayor en las células SNU1 que en las KATO III. Por lo tanto, concluimos que el efecto citotóxico (en términos de pérdida de viabilidad celular determinada por MTS) de QS-21 y QA no estaba relacionado exclusivamente con su capacidad de alterar las membranas (como demuestra la prueba de viabilidad celular basada en la liberación de LDH). Este hallazgo fue prometedor y nos llevó a investigar si los mecanismos apoptóticos estaban implicados en la pérdida de viabilidad observada (como alteración metabólica) de ambos tipos de células tumorales tras la exposición a dosis medias o bajas de QS-21 y QA.
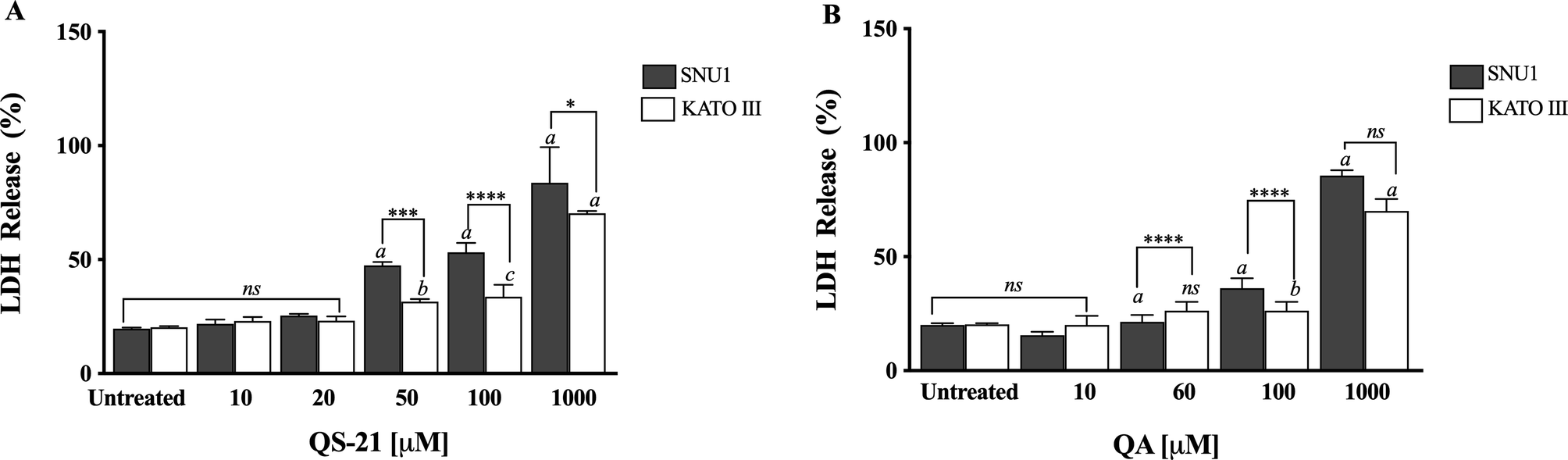
Figura 3. Análisis de la actividad de la LDH. Los resultados se expresan como porcentaje de liberación de LDH menos el valor de control del vehículo. a, b y c indican un P <0.0001, P<0,01 y P<0,05, respectivamente, cuando se compara SNU1 y KATO III con células no tratadas, ****, *** y * indican un P<0.0001, P<0,005 y P<0,05 entre SNU1 frente a KATO III tratadas con QS-21 (A) o QA (B) y ns (no significativo) entre líneas celulares. Los puntos de datos son valores medios ± DE de tres experimentos independientes, cada uno realizado por triplicado.
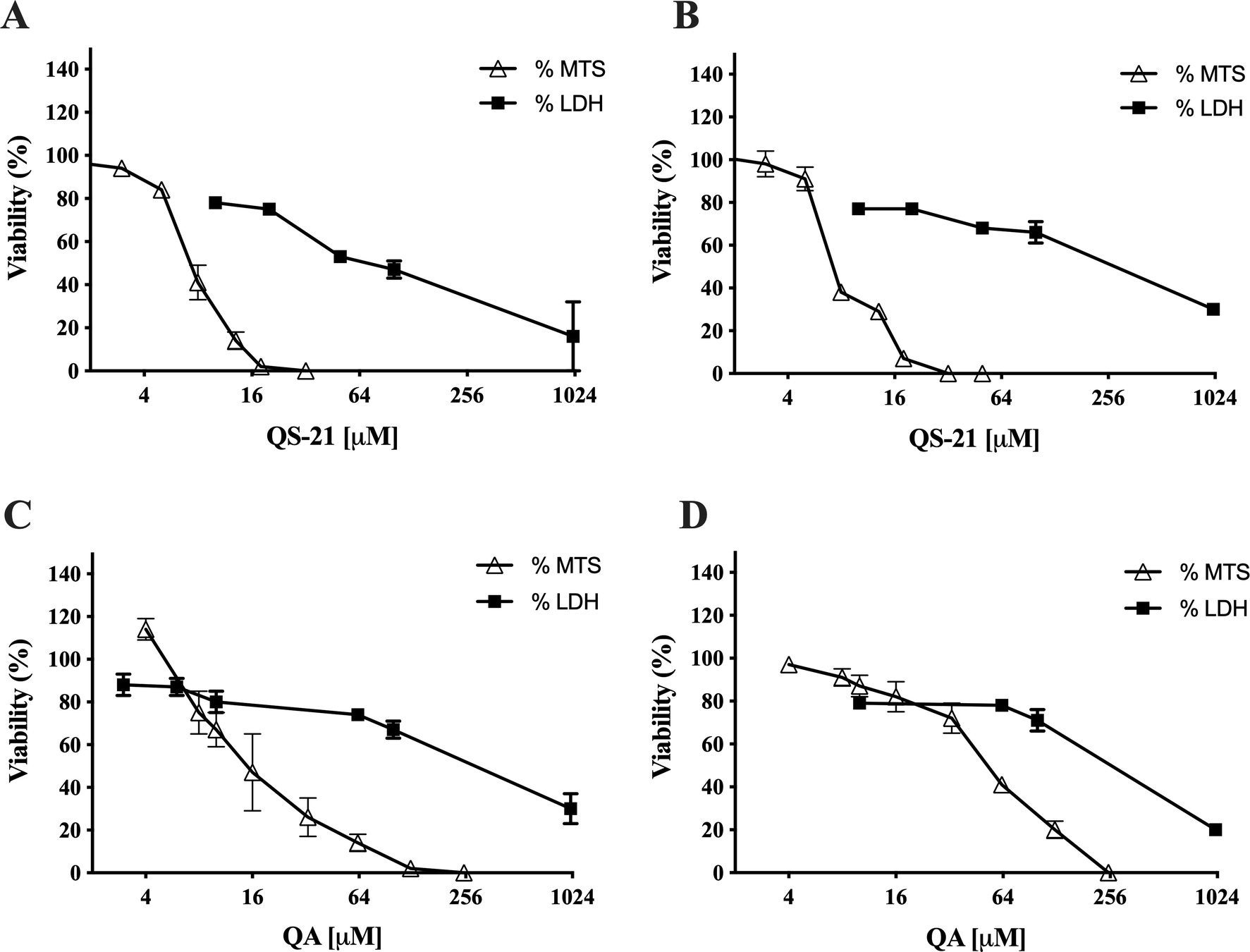
Figura 4. Correlación entre los ensayos MTS y LDH. Comparación del efecto de QS-21 y QA sobre la viabilidad metabólica (determinada por MTS) y la viabilidad en términos de integridad de la membrana (determinada por la liberación de LDH) de las células SNU1 y KATO III. (A) y (B) QS-21 sobre SNU1 y KATO III, respectivamente. (C) y (D) QA en SNU1 y KATO III, respectivamente.
Evaluación del efecto de las fracciones QS-21 y QA sobre el daño del ADN y la inducción de caspasas
Cuando se incubaron células SNU1 con 10 µM de QS-21 durante 24 h, se produjo un 82% (P<0,0001) de células TUNEL positivas en comparación con las células no tratadas, como se muestra en la Fig. 5A, C, mientras que la incubación con 100 µM de QA alcanzó un 36% (P <0,005) de células TUNEL positivas (Fig. 5C, D). El efecto de QA a 100 µM sobre las células KATO III dio lugar a porcentajes bajos de daño del ADN que alcanzaron el 15% (P<0,005), como se muestra en la Fig. 5D. El tratamiento de las células KATO III con QS-21 (10 μM) mostró un efecto destacado en la inducción de la apoptosis celular, generando un 50% (P<0,0001) de células TUNEL positivas (Fig. 5B, D). Curiosamente, observamos que QS-21 es más eficaz que QA y STS para desencadenar la fragmentación del ADN en SNU1 y KATO III. Para confirmar este resultado obtenido mediante el ensayo TUNEL, empleamos la citometría de flujo utilizando Annexin V y 7-aminoactinomicina D. Los resultados de la apoptosis se muestran en la Fig. 6, donde el porcentaje de células SNU1 sometidas a muerte celular apoptótica aumentó hasta el 42% y el 72% para QA y QS-21, respectivamente, en comparación con las células no tratadas. En el caso de KATO III, tras la exposición a 100 μM de QA o 10 μM de QS-21 alcanzó el 73% y el 49%, respectivamente (Fig. 6). Por último, comprobamos la inducción de las caspasas 3/7 en ambas líneas celulares tumorales con 10 µM de QS-21 y 100 µM de QA durante 24 h, lo que produjo una inducción significativa de la actividad de las caspasas 3/7 en comparación con el control negativo (P<0,0001), como se observa en la Fig. 7.
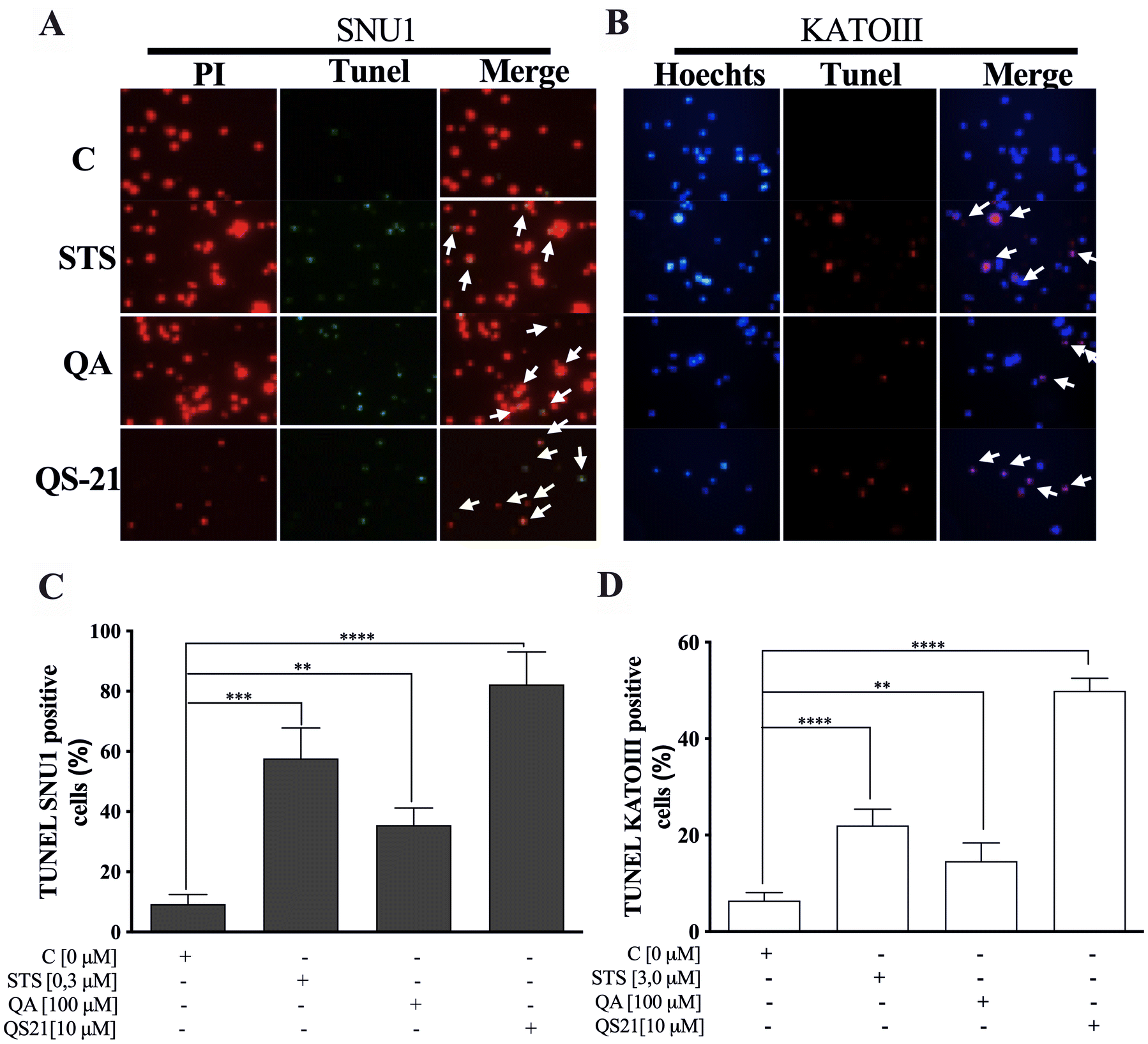
Figura 5. QS-21 y QA inducen la apoptosis por fragmentación del ADN (ensayo TUNEL) en SNU1 y KATO III. (A) y (B) son imágenes representativas de la tinción TUNEL. Las células TUNEL positivas (fluorescencia verde brillante, Fluoresceína 12-dUTP) con el kit DeadEnd Fluorometric TUNEL y TUNEL positivas (fluorescencia roja) con Click-iT TUNEL Alexa Fluor 594, se observaron tras el tratamiento de 1 × 105 células con 10 μM QS-21 y 100 μM QA, respectivamente. Como control negativo se utilizaron células no tratadas y como control positivo células tratadas con 0,3 y 3,0 μM de STS. Todas las células SNU1 se tiñeron con PI (fluorescencia roja) y las células KATO III se tiñeron con Hoechst 33342 (fluorescencia azul). Las flechas blancas indican las células apoptóticas. (C) **P<0,005, ***P<0,0005 y ****P<0,0001 células tratadas con SNU1 frente al grupo de control; (D) **P<0,005 y ****P<0,0001 células tratadas con KATO III frente al grupo de control. En cada experimento se examinaron ocho campos con un aumento de × 400 y todos los datos se muestran como media ± DE de tres experimentos distintos.
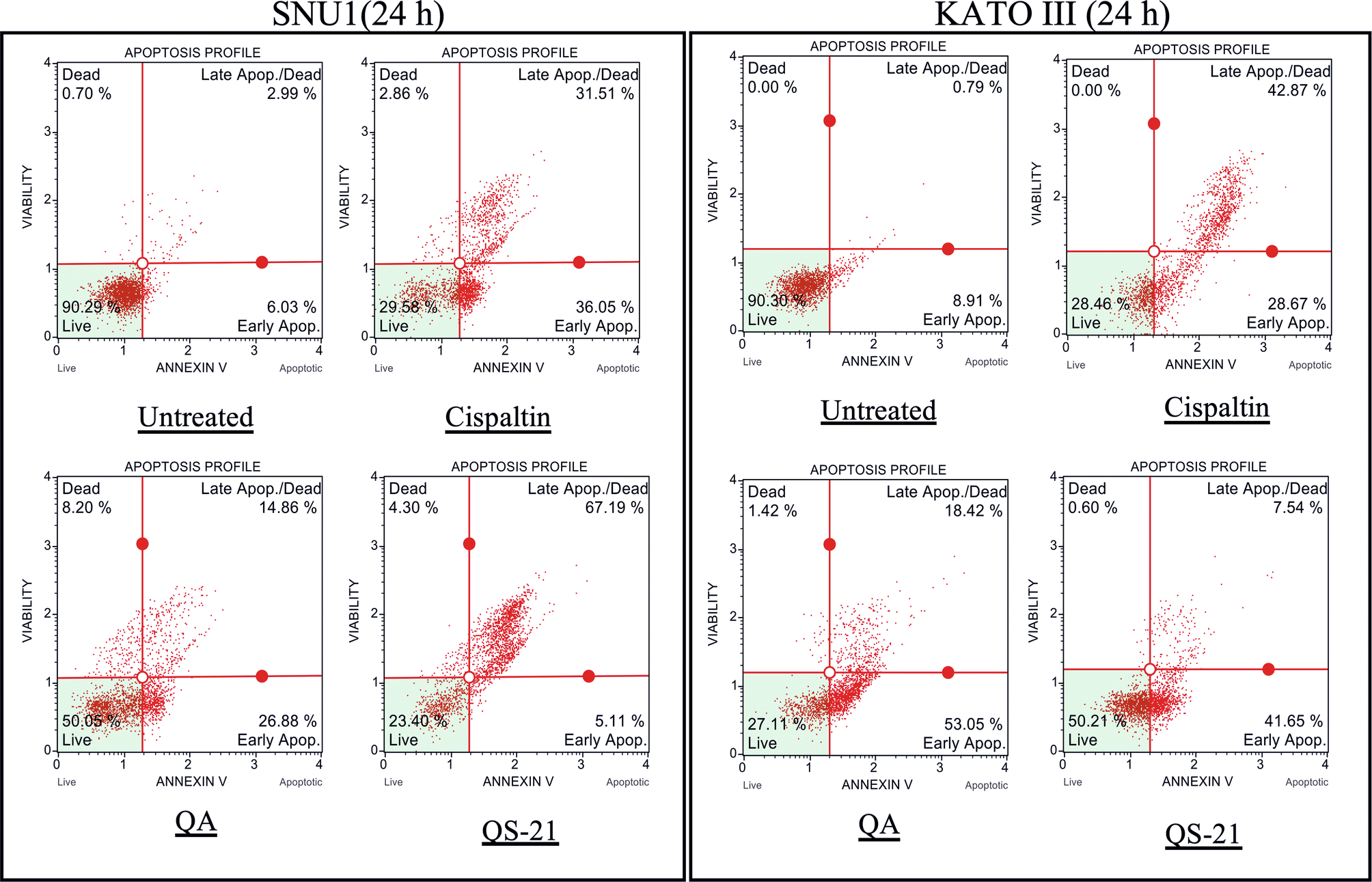
Figura 6. QS-21 y QA inducen la apoptosis en SNU1 y KATO III. Se trataron 1 × 105 células con QS-21 (10 μM) o QA (100 μM) durante 24 h y se determinó la distribución de las células apoptóticas mediante citometría de flujo. Se estimó el porcentaje de células apoptóticas tempranas y tardías (tasa de apoptosis) en comparación con la célula no tratada y como control positivo se trataron las células con Cisplatino (55 μM). SNU1 (panel izquierdo) y KATO III (panel derecho).
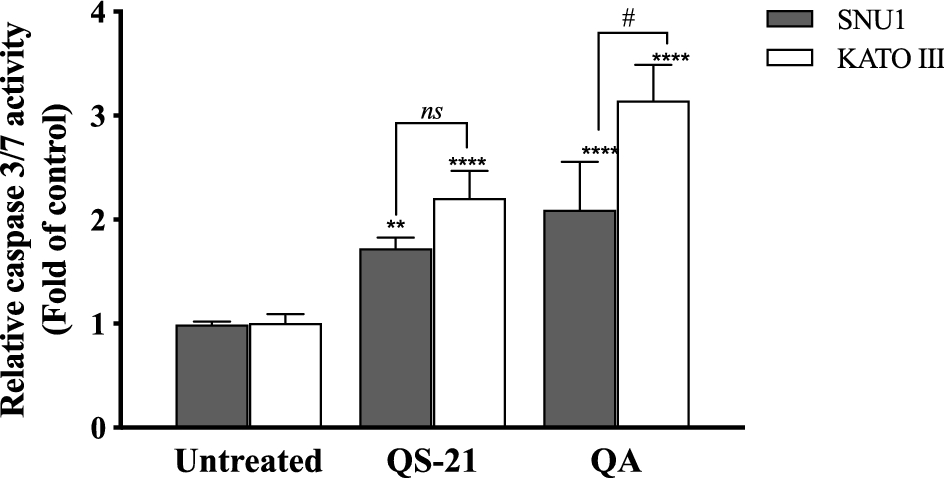
Figura 7. QS-21 y QA inducen la actividad de la caspasa 3/7 en SNU1 y KATO III. Se trataron aproximadamente 2 × 104 células con QS-21 (10 µM) o QA (100 μM) durante 24 h. Se midió la Caspasa-Glo 3/7 mostrando que QS-21 y QA inducían la actividad de la caspasa 3/7 en ambas líneas celulares. Columnas, media (n = 5); barras, DE. ****o # P<0,0001; ** P<0,005 y ns no significativo.
Características fisicoquímicas in silico y acoplamiento molecular
La Tabla 2 muestra las energías de unión predichas (ΔGbinding) para los compuestos en complejo con un conjunto de proteínas relacionadas con el cáncer con estructura 3D conocida sobreexpresadas en varias líneas celulares de cáncer, las líneas celulares SNU1 y KATO III. Entre las proteínas mencionadas, tanto el QS-21 como el QA se unen más fuertemente a la proteína proapoptótica BID (entrada PDB: 2BID) que a otras proteínas, con valores de ΔGbinding – 8,2 y – 9,9 kcal/mol, respectivamente.
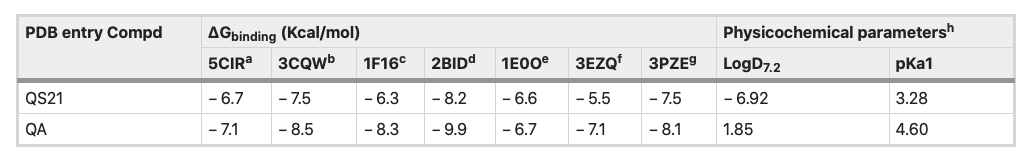
Tabla 2. Energías libres de enlace y parámetros in silico de QS-21 y QA. aReceptor de muerte 4 (DR4), bAKT1, cproteína apoptótica BAX, dproteína apoptótica BID, eFGFR2, fproteína FAS y gJNK1. hLos datos in silico se calcularon con el software MarvinSketch (versión 18.24.0, ChemAxon Ltd.).
La figura 8 representa el sitio de unión potencial y la pose de QS-21 y QA acoplados en 2BID, donde se puede observar que ambos compuestos se encuentran en la misma cavidad de unión de 2BID. Sin embargo, QS-21 y QA difieren tanto en orientación como en conformación en el sitio de unión, lo que conduce a una interacción selectiva de cada compuesto con residuos aminoácidos específicos del sitio de unión. Las interacciones de cada compuesto con el bolsillo de unión del 2BID se rigen principalmente por enlaces de hidrógeno e interacciones hidrofóbicas. Los aminoácidos responsables del enlace de hidrógeno de 2BID con QS-21 son Gly43, Asp73, Glu82 y Arg86, mientras que con QA son Asn33 y Leu39 (Fig. 8B). Por otra parte, los aminoácidos responsables de los contactos hidrófobos con QS-21 son Phe24 y Trp53, mientras que con QA es Leu39 (Fig. 8C). Además, como se muestra en la Tabla 2, se determinaron los valores logD y pKa de los compuestos. QS-21 y QA mostraron valores de pKa 3,28 y 4,60, respectivamente. Estos resultados indican que ambos compuestos deberían encontrarse principalmente como sus respectivas formas aniónicas a un pH fisiológico (~ 7,4). Además, QS-21 y QA mostraron los valores LogD7.2 – 6,92 y 1,85, respectivamente, lo que indica que QS-21 es un compuesto hidrófilo y QA es un compuesto hidrófobo.
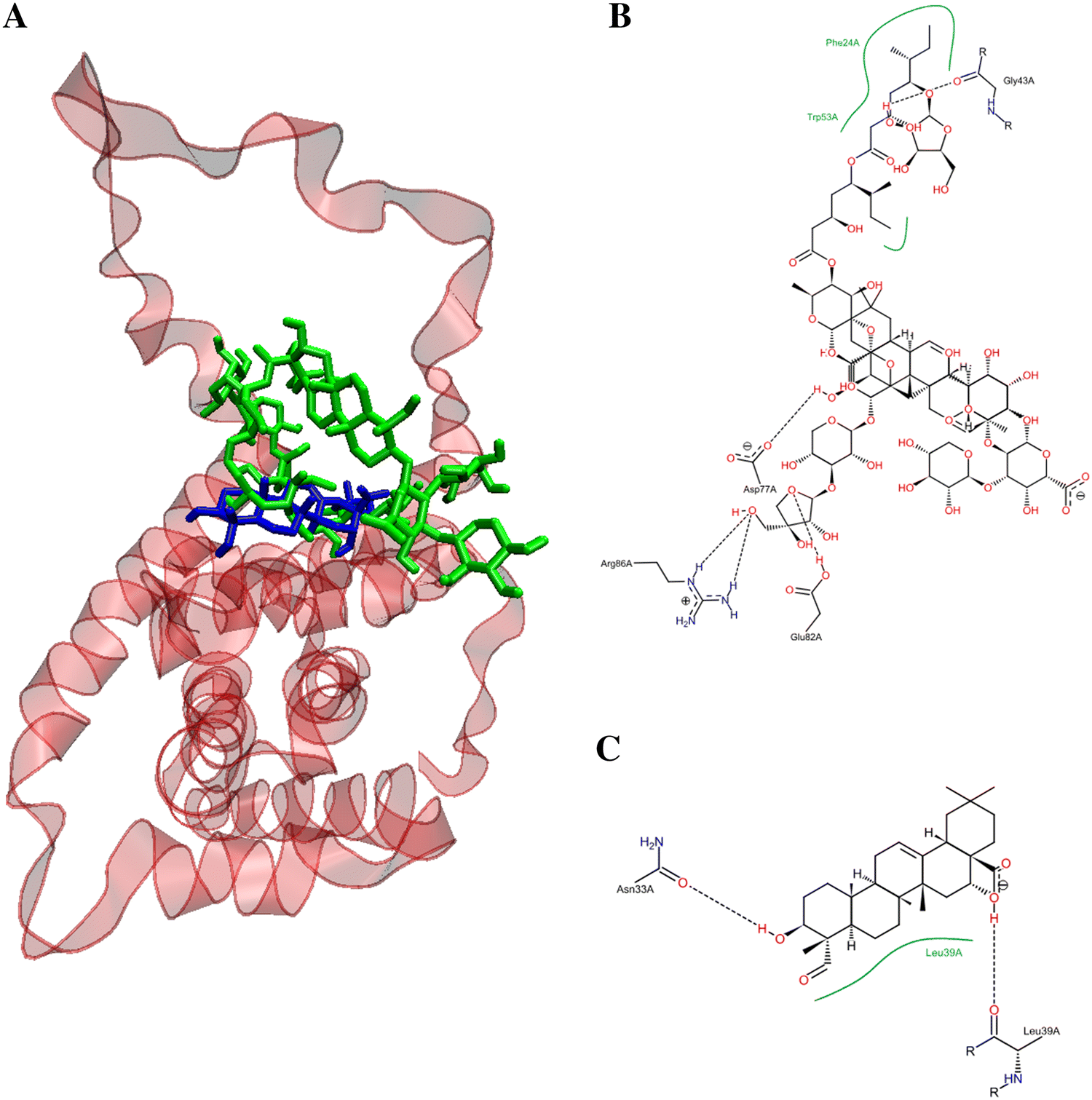
Figura 8. Sitio de unión potencial para la pose de menor energía de QS-21 y QA acoplados dentro de la proteína proapoptótica BID (entrada PDB: 2BID). (A) Representación en cinta de la 2BID con los ligandos dentro del sitio activo. QS-21 y QA están coloreados en verde y azul, respectivamente. Una inspección detallada del sitio de unión dentro de la 2BID muestra los aminoácidos responsables de la interacción con QS-21 (B) y QA (C).
Debate
En el presente estudio, demostramos que QS-21 y su aglicona QA de Q. saponaria ejercen un efecto citotóxico en función de la dosis contra las líneas celulares SNU1 y KATO III mediante el ensayo MTS. Además, QS-21 y QA tienen un mejor efecto sobre las células SNU1 que sobre las KATO III. Además, estos compuestos tienen un efecto bajo sobre la permeabilidad de la membrana celular evaluada mediante el ensayo de liberación de LDH. De hecho, los resultados de la LDH indican que la alteración metabólica se produjo sin causar pérdida en la integridad de la membrana. Teniendo en cuenta lo anterior, confirmamos, mediante ensayos de TUNEL, Annexin V y caspasas, que QS-21 y QA desencadenan un proceso de apoptosis, en el que QS-21 fue más eficaz para inducir la apoptosis en SNU1 que en KATO III.
Según el índice de hidrofobicidad calculado, QA (valor LogP de 1,85) podría atravesar fácilmente la membrana celular, mientras que QS-21 es el menos probable debido a su menor índice de hidrofobicidad (valor LogP de – 6,92). Por lo tanto, estos resultados (viabilidad y liberación de LDH) estarían explicando por qué estos compuestos tienen una respuesta diferente en las células SNU1 y KATO III. De hecho, los estudios han demostrado que las saponinas triterpenoides y sus agliconas son capaces de inhibir la proliferación y de inducir la muerte por apoptosis en varias líneas celulares cancerosas mediante un efecto lítico por permeabilización de las membranas o por una interacción con la membrana plasmática12,13. Las pruebas indican que la reorganización de las balsas lipídicas con Avicin D, otra saponina triterpenoide vegetal, estaría implicada en la supervivencia o muerte celular13,14,15,16. Por lo tanto, la QS-21 también podría desencadenar la apoptosis celular mediante la reordenación de las balsas lipídicas de la membrana celular o induciendo la trimerización de DR4 o FAS16,17. Los resultados del acoplamiento mostraron que el QS-21 se une más fuertemente al receptor DR4 que al receptor FAS, como se muestra en la Tabla 2. Además, nuestros resultados de acoplamiento también mostraron que QS-21 y QA tienen mayor afinidad de unión a la proteína proapoptótica BID, por lo que estos compuestos podrían estar implicados en la inducción de la apoptosis a través de la proteína proapoptótica, además de la activación de caspasas como la saikosaponina D en los hepatocitos17. Curiosamente, nuestros estudios de acoplamiento muestran que la QS-21 interactúa con el dominio BH3 de la proteína proapoptótica BID, al igual que los agentes anticancerígenos estándar como el venetoclax, el obatoclax, el navitoclax y la prodigiosina18,19,20. El dominio BH3 es una región conservada en los miembros de la familia Bcl-2 y crítica para iniciar la apoptosis21,22. Aunque QA y QS-21 comparten el mismo bolsillo de unión en la proteína BID, difieren tanto en orientación como en conformación al interactuar selectivamente con residuos específicos del sitio de unión, incluidos los aminoácidos responsables del enlace de hidrógeno (ver Fig. 8), porque ambos compuestos tienen tamaños moleculares diferentes debido a los azúcares presentes en la estructura de QS-21.
Nuestro estudio ha demostrado que la QS-21 tiene efecto citotóxico sobre las células de cáncer gástrico humano, mostrando valores de IC50 en torno a 7,4 µM para SNU1 y KATO III, casi 3 veces mejor que los estudios anteriores con saponina triterpenoide extraída de las raíces de Adenophora triphylla var. japonica23,24. Este hallazgo sugiere que la presencia del grupo acilo en la posición C28 podría proporcionar una mayor citotoxicidad a la QS-21. Mientras que QA mostró valores de IC50 para SNU1 y KATO III en un rango similar (5-100 µM) al descrito con agliconas triterpenoides en diferentes líneas de células tumorales7,24,25,26. Además, ambos compuestos fueron selectivos contra las células tumorales gástricas sin afectar a la proliferación de las células GES-1, como se muestra en la Fig. 2 y la Tabla 1.
En conclusión, nuestros hallazgos sugieren que el QS-21 y su aglicona QA tienen una importante actividad selectiva antitumoral in vitro contra las células de cáncer gástrico humano, SNU1 y KATO III, induciendo la muerte celular mediante un mecanismo apoptótico que implica la actividad de las caspasas y la fragmentación del ADN. Sin embargo, en términos de los perfiles IC50 obtenidos con ambos compuestos, QS-21 demostró ser un agente antitumoral más potente que QA. Es importante señalar que para confirmar estos estudios in vitro y nuestros estudios de acoplamiento, sería necesario evaluar en un futuro el mecanismo implicado en la generación de la muerte celular, es decir, si QS-21 induce la muerte celular a través de la vía extrínseca o intrínseca y evaluar si QA tienen capacidad para atravesar la membrana celular, desencadenando la muerte celular. Además, sería muy interesante evaluar la actividad antiproliferativa de la QS-21 y la QA en otras líneas celulares cancerosas.
Materiales y métodos
Líneas celulares
Las líneas celulares humanas de GC (SNU1 y KATO III) se obtuvieron de la American Type Culture Collection ATCC (Manassas, VA, EE.UU.) y se mantuvieron en RPMI 1.640 suplementado con un 10% de FBS, penicilina 100 U/mL y estreptomicina 100 μg/mL. Como control sano se utilizó la línea celular epitelial gástrica humana (GES-1), mantenida en medio DMEM (amablemente donado por el Dr. Dawit Kidane-Mulat de la Universidad de Texas-Austin).
Ensayos celulares
Ensayo MTS Ensayo de proliferación CellTiter 96 AQueous One Solution, sistema TUNEL fluorométrico Dead End y ensayo Caspase-Glo 3/7 adquiridos a Promega, (Madison, WI, EE.UU.). Click-it TUNEL Alexa Fluor 594 de Life Technologies. Ensayo de células muertas y anexina V de Muse (Merck, Millipore, EE.UU.). LDH-Cytotoxicity Assay se adquirió a Thermo Scientific (Thermo, Waltham, MA, EE.UU.). La estaurosporina (STS), el yoduro de propidio (PI) y el cisplatino se obtuvieron de Sigma-Aldrich (St. Louis, MO, EE.UU.). Los medios de cultivo celular (RPMI1640, DIMEN) y el suero bovino fetal inactivado por calor (FBS), así como los antibióticos (penicilina y estreptomicina) se adquirieron a Corning CellGro (Nueva York, NY, EE.UU.).
Compuestos triterpénicos
Las muestras de QS-21 y QA fueron suministradas por Desert King International (CA, EE.UU.). El QS-21 se purificó a partir de un extracto altamente purificado de la corteza de Q. saponaria (SuperSap, Desert King International). El extracto se fraccionó mediante HPLC preparativa de fase inversa en una columna de octadecilsilano eluida con un gradiente de agua acidificada y acetonitrilo siguiendo un enfoque general descrito en otro lugar 6. Las fracciones que contenían QS-21 se agruparon y liofilizaron, obteniéndose la fracción QS-21 empleada en este estudio. La QA se preparó mediante hidrólisis ácida del extracto altamente purificado de Q. saponaria (VaxSap, Desert King International, CA, EE.UU.), siguiendo un procedimiento general descrito en otro lugar por Rodríguez-Díaz et al.27. Para las pruebas biológicas de QS21 y QA, se preparó una solución madre de cada compuesto en dimetilsulfóxido (DMSO) (2,5 mM y 0,1 mM, respectivamente).
Prueba de la actividad citotóxica mediante la prueba MTS
Se sembraron SNU1, KATO III y GES-1 (5 × 105 células/pocillo) en una placa de 96 pocillos en el medio respectivo y se incubaron durante 24 h a 37 °C en una atmósfera humidificada con un 5% de CO2 para recuperar las células. Se probaron ambos compuestos durante 24 h; QS-21 (0-50) µM en células SNU1, KATO III y GES-1, respectivamente; QA (0-250) µM en células SNU1, KATO III y GES-1, respectivamente. El STS, un inhibidor de la proteína cinasa, se utilizó como control positivo de la muerte en las líneas celulares SNU1 y KATO III determinada mediante el ensayo MTS, utilizando las concentraciones descritas en la bibliografía28,29 (Material suplementario S1). El ensayo MTS se realizó según las instrucciones del fabricante. A continuación, se registró la absorbancia a 490 nm utilizando un lector ELISA Epoch (ELx800, BioTek, VT, EE.UU.). Las células tratadas con DMSO 0,2% o PBS se incluyeron como control del vehículo. La viabilidad celular (expresada como porcentaje de la viabilidad de las células no expuestas a QS-21o QA). El experimento se realizó por triplicado. Se determinaron los valores IC50 para QS-21 y QA.
Evaluación de la actividad citotóxica mediante la liberación de la enzima lactato deshidrogenasa (ensayo LDH)
El efecto citotóxico de ambos compuestos triterpénicos sobre la integridad de la membrana celular se determinó detectando la liberación de LDH al medio extracelular. Se sembraron 3 × 105 células/pocillo (SNU1 y KATO III) en una placa negra de 96 pocillos con RPMI 1.640 como se ha descrito anteriormente. Cada compuesto triterpénico se añadió a las suspensiones celulares a las siguientes concentraciones: (1) QS-21, 0-12 µM; (2) QA, 0-125 µM. El ensayo de citotoxicidad de la LDH se realizó según las instrucciones del fabricante. La absorbancia se midió a 490 nm y 680 nm utilizando un lector ELISA Epoch (ELx800, BioTek, VT, EE.UU. un espectrofotómetro de lectura en placa para determinar la actividad de la LDH. La citotoxicidad se expresó en porcentaje. El experimento se realizó por triplicado.
Ensayo de tinción TUNEL
Se sembraron 1 × 105 células de SNU1 y KATO III en una placa de 35 mm como se ha descrito anteriormente. A continuación, se añadieron a las células QS-21 (10 µM), QA (100 µM) o STS (control positivo de la apoptosis celular); la concentración de STS en cada ensayo fue de 0,3 µM (SNU1) y 3,0 µM (KATO III), y se incubaron durante 24 h en las condiciones anteriores (figura suplementaria S1). Las células SNU1 se analizaron utilizando el kit del sistema TUNEL fluorométrico Dead End según las instrucciones del fabricante. Las células KATO III se analizaron utilizando el kit Click-it TUNEL Alexa Fluor 594. El motivo de utilizar un kit diferente fue la elevada fluorescencia de fondo inespecífica con el primer kit. Brevemente, las células SNU1 y KATO III incubadas se fijaron, permeabilizaron y marcaron con fluoresceína 12-dUTP y Alexa Fluor 594, respectivamente. Este paso se realizó en un microscopio de fluorescencia Nikon H550L equipado con filtros de fluorescencia estándar ajustados a: (1) 520 nm para visualizar las células SNU1 apoptóticas marcadas con Fluoresceína-12-dUTP (fluorescencia verde); (2) 460 nm para visualizar todas las células SNU1 teñidas con Yoduro de propidio (PI: fluorescencia roja); (3) 590 nm para visualizar las células apoptóticas KATO III teñidas con Alexa Fluor 594 (fluorescencia roja), y (4) 490 nm para visualizar la fluorescencia azul de todas las células KATO III teñidas con Hoechst 33342. Las células se fotografiaron en 8 campos diferentes con un aumento de 400X.
Ensayo de anexina V
Se sembraron 2 × 105 células de SNU1 y KATO III en placas de 6 pocillos como se ha descrito anteriormente. A continuación, las células SNU1 y KATO III se suplementaron con QS-21 (5 µM) o QA (100 µM). Se utilizó cisplatino (55 µM) como control positivo y células no tratadas como control negativo. Todos los ensayos se incubaron durante 24 h. Tras la incubación, las células se lavaron con 1 mL de PBS y se añadieron 100 µL del reactivo Muse Annexin V& Dead Cell. La apoptosis se midió con el analizador celular Muse y el software de análisis Muse (Merck-Merck Millipore) y las células se clasificaron en cuatro grupos: vivas, apoptóticas tempranas, apoptóticas tardías y muertas o necróticas.
Ensayo de la actividad de las caspasas
Se sembraron 2 × 104 células (SNU1 y KATO III) en placas de 96 pocillos como se ha descrito anteriormente. A continuación, las células se suplementaron con QS-21 (5 µM) o QA (100 µM), y se incubaron durante 24 h. Las actividades de las caspasas 3 y 7 tras la incubación de las células se detectaron mediante el ensayo Caspase-Glo 3/7 siguiendo las instrucciones del fabricante. La fluorescencia de los lisados (proporcional a la cantidad de actividad de las caspasas presente) se midió a 510 nm en un lector de placas de fluorescencia multipocillo Appliskan (Thermo Fischer Scientific, Waltham, MA, EE.UU.).
Predicción in silico de parámetros fisicoquímicos y acoplamiento molecular
La estructura 2D de QA (CID: 101.810) y QS-21 (CID: 73.652.135) se recuperó en formato de archivo SDF de la base de datos PubChem del NCBI (https://pubchem.ncbi.nlm.nih.gov). Estas moléculas se visualizaron y sus valores de pKa y LogD se calcularon con el software Marvin Sketch (versión 18.24.0, ChemAxon Ltd.). Las concentraciones de Cl- y Na+ K+ se fijaron en 0,108 mol/L y 0,133 mol/L, respectivamente, para el cálculo del logD. Para el cálculo de pKa y LogD se tuvo en cuenta la tautomerización para QA y QS-21.
Recurrimos al cribado virtual utilizando Autodock Vina, un método de puntuación de dianas específicas útil para el cribado virtual30. QS-21 y QA se acoplaron a un conjunto de bolsillos de proteínas para identificar la proteína diana que podría ser inhibida potencialmente por estos compuestos. Aquí realizamos un acoplamiento rígido tomando todo el receptor para identificar los posibles bolsillos de unión de las proteínas. La estructura cristalina de las proteínas, incluidas las enzimas, el factor de crecimiento, los receptores y la proteína proapoptótica, se recuperó del Banco de Datos de Proteínas (PDB)31,32 utilizando los ID PDB 5CIR, 3CQW, 1F16, 2BID, 1E0O, 3EZQ y 3PZE (ver más información en la Tabla 2). Tanto los ligandos como las proteínas se prepararon utilizando AutoDock Tools versión 1.5.6 (ADT), como se ha descrito previamente32. Por último, el análisis gráfico de los estudios de acoplamiento molecular se realizó con VMD33.
Procesamiento de datos y análisis estadístico
Los resultados se expresaron como media ± desviación estándar (DE). Los datos se analizaron mediante análisis de dos vías y de una vía (ANOVA) con la prueba de comparaciones múltiples de Tukey (P<0,005) utilizando GraphPad Prism 8 (GraphPad Software, San Diego, CA, EE.UU.).
Referencias
1. Luo, G. et al. Patrones y tendencias mundiales en la incidencia del cáncer de estómago: Análisis por edad, periodo y cohorte de nacimiento. Int. J. Cancer Glob. 141, 1333-1344 (2017).
2. Housman, G. et al. Resistencia a los fármacos en el cáncer: Una visión general. Cánceres (Basilea). 6, 1769-1792 (2014).
3. Czajkowska, A. et al. Efecto anticancerígeno de un nuevo derivado y su acción sinérgica con Nigella sativa en células humanas de cáncer gástrico. Biomed. Res. Int. 2017, 1-13 (2017).
4. Moses, T. & Papadopoulou, K. K. Diversidad metabólica y funcional de las saponinas, intermediarios biosintéticos y derivados semisintéticos. Crit. Rev. Biochem. Mol. Biol. 49, 1-24 (2014).
5. Guo, S., Falk, E., Kenne, L., Ro, B. & Sundquist, B. G. Saponinas triterpenoides que contienen un residuo acetilado de fucosilo ramificado de Quillaja saponaria Molina. Fitoquímica 53, 861-868 (2000).
6. Kensil, C. R., Patel, U., Lennick, M. & Marciani, D. Separación y caracterización de saponinas con actividad adyuvante procedentes de la corteza de Quillaja saponaria Molina. J. Immunol. 146, 431-437 (1991).
7. Wang, Y. et al. El extracto de planta natural Tubeimoside I promueve la muerte celular mediada por apoptosis en células cultivadas de hepatoma humano (HepG2). Biol. Pharm. Bull. 34, 831-838 (2011).
8. Kaufmann, T., Strasser, A. & Jost, P. J. Señalización del receptor de muerte Fas: Roles de Bid y XIAP. Muerte Celular Difer. 19, 42-50 (2012).
9. Guicciardi, M. E. & Gores, G. J. Vida y muerte por receptores de muerte. FASEB J. 23, 1625-1637 (2009).
10. Kunii, K. et al. Las líneas celulares de cáncer gástrico amplificadas por FGFR2 requieren la señalización de FGFR2 y Erbb3 para su crecimiento y supervivencia. Cancer Res. 68, 2340-2348 (2008).
11. Gavrieli, Y., Sherman, Y. & Ben-Sasson, S. A. Caracterización de la reducción celular del bromuro de 3-(4, 5-dimetiltiazol-2-il)-2,5-difeniltetrazolio (MTT): Localización subcelular, dependencia del sustrato e implicación del transporte mitocondrial de electrones en la reducción del MTT. Arch. Biochem. Biophys. 303, 474-482 (1992).
12. Podolak, I., Galanty, A. & Sobolewska, D. Las saponinas como agentes citotóxicos: Una revisión. Fitoquímica. Rev. 9, 425-474 (2010).
13. George, K. S. & Wu, S. Balsa de lípidos: Una isla flotante de muerte o supervivencia. Toxicol. Farmac. Aplic. 259, 311-319 (2012).
14. Tsai, C. et al. Efecto de la saponina de soja en el crecimiento de células de cáncer de colon humano. World J. Gastroenterol. 16, 3371-3376 (2010).
15. Li, J. et al. La saponina 1 induce la apoptosis y suprime la señalización de supervivencia mediada por NF-κB en el glioblastoma multiforme (GBM). PLoS ONE 8, e81258 (2013).
16. Xu, Z. X., Ding, T., Haridas, V., Connolly, F. & Gutterman, J. U. La avicina D, un triterpenoide vegetal, induce la apoptosis celular mediante el reclutamiento de Fas y moléculas de señalización descendentes en balsas lipídicas. PLoS ONE 4, e8532 (2009).
17. Zhang, F. et al. La activación de la vía del receptor de muerte Fas y Bid en los hepatocitos está implicada en la inducción de hepatotoxicidad por saikosaponina D. Toxicol. Toxicol. Pharmacol. 41, 8-13 (2016).
18. Interacciones moleculares de las prodigininas con el dominio BH3 de los miembros antiapoptóticos de la familia Bcl-2 . PLoS ONE 8, 1-8 (2013).
19. Chen, G. et al. A natural chalcone induces apoptosis in lung cancer cells: 3D-QSAR, docking and an in vivo/vitro assay. Rep. Sci. Rep. 7, 1-10 (2017).
20. Ramos, J., Muthukumaran, J., Freire, F., Paquete-ferreira, J. & Santos-silva, T. Shedding light on the interaction of human anti-apoptotic Bcl-2 protein with ligands through biophysical and in silico studies. Int. J. Mol. Sci. Artic. 20, 860-872 (2019).
21. Chittenden, T. Dominios BH3: Ligandos de muerte intracelulares críticos para iniciar la apoptosis. Cell Press. 2, 165-166 (2002).
22. Huang, Z. La biología química de la apoptosis: Revisión que explora las interacciones proteína-proteína y la vida y muerte de las células con pequeñas moléculas. Quím. Biol. 9, 1059-1072 (2002).
23. Chun, J., Kang, M. & Kim, Y. S. Una saponina triterpenoide de la Adenophora triphylla var. japonica suprime el crecimiento de las células de cáncer gástrico humano mediante la regulación de la apoptosis y la autofagia. Tumor Biol. 35, 12021-12030 (2014).
24. Lu, Y., Van, D., Deibert, L., Bishop, G. & Balsevich, J. Fitoquímica antiproliferativa del ácido quilláico y las saponinas gipsogeninas de las raíces de Saponaria officinalis L. Fitoquímica 113, 108-120 (2015).
25. Kikuchi, T. et al. El ácido 3-O-(E)-p-cumaroyl tormentic de las hojas de Eriobotrya japonica induce la muerte celular apoptótica dependiente de caspasas en la línea celular de la leucemia humana. Quím. Pharm. Bull. 59, 378-381 (2011).
26. Panucci, R. K. I., Oliveira, C. R., de Mello Marin, W. & Bincoletto, C. Estudio in vitro del potencial antileucémico del ácido ursólico en la línea celular Jurkat. J. Clin. Exp. Oncol. 5, 3 (2016).
27. Rodríguez-díaz, M., Delporte, C., Cartagena, C. & Wessjohann, L. A. Actividad antiinflamatoria tópica del ácido quiláico de Quillaja saponaria Mol. y algunos derivados. Farmac. Pharmacol. 3, 718-724 (2011).
28. Pregi, N., Vittori, D., Pérez, G., Leirós, C. P. & Nesse, A. Efecto de la eritropoyetina sobre la apoptosis inducida por estaurosporina y la diferenciación de las células de neuroblastoma SH-SY5Y. Biochim. Biophys. Acta 1763, 238-246 (2006).
29. Antonsson, A. & Persson, J. L. La inducción de la apoptosis por la estaurosporina implica la inhibición de la expresión de las principales proteínas del ciclo celular en el punto de control G2/M, acompañada de alteraciones en las actividades de las cinasas Erk y Akt. Anticancer Res. 29, 2893-2898 (2009).
30. Trott, O. & Olson, A. J. AutoDock Vina: Mejora de la velocidad y precisión del docking con una nueva función de puntuación, optimización eficiente y multihilo. J. Comput. Chem. 31, 455-461 (2009).
31. Berman, H. M. et al. El banco de datos de proteínas. Nucleic Acids Res. 28, 235-242 (2000).
32. Molinari, A. et al. Benzoindazolequinonas antiproliferativas como inhibidores potenciales de la ciclooxigenasa-2. Molecules 24, 1-17 (2019).
33. Humphrey, W., Dalke, A. & Schulten, K. V. M. D. Dinámica molecular visual. J. Mol. Graf. 14, 33-38 (1996).
Agradecimientos
Agradecemos especialmente al Dr. Dawit Kidane-Mulat (Universidad de Texas -Austin) que donó las células GES-1 (línea celular de epitelio gástrico normal). Damos las gracias a Hugo Verli y Conrado Pedebos (Biotecnología de la Universidad de Federal do Rio Grande do Sul), por facilitarnos la estructura tridimensional de QS-21. Con el apoyo de la Dirección de Investigación de la Vicerrectoría de Investigación y Estudios Avanzados. Pontificia Universidad Católica de Valparaíso, Chile [DI0 .37-274/DI037.227], DESERT KING Chile, CONICYT-FONDAP 15130011, CONICY-Becas N°21141206/Nº 21151252.
Información del autor
Afiliaciones
Laboratorio de Química Biológica, Instituto de Química, Facultad de Ciencias, Pontificia Universidad Católica de Valparaíso, Valparaíso, Chile
Leda Guzmán, Katherine Villalón, María José Marchant, María Elena Tarnok, Pilar Cárdenas, Gisela Aquea & Waldo Acevedo
Natural Response S.A, Av. Industrial 1970, Quilpué, Región de Valparaíso, Chile
Leandro Padilla
Laboratorio de Biología Molecular y Celular del Cáncer, Departamento de Ciencias Biomédicas, Facultad de Medicina, Universidad Católica del Norte, Coquimbo, Chile
Giuliano Bernal
Laboratorio de Química Orgánica, Instituto de Química, Facultad de Ciencias, Pontificia Universidad Católica de Valparaíso, Valparaíso, Chile
Aurora Molinari
Laboratorio de Oncología, Departamento Hematología y Oncología, Facultad de Medicina, Pontificia Universidad Católica de Chile, Santiago, Chile
Alejandro Corvalán
Centro Avanzado de Enfermedades Crónicas, Santiago, Chile
Alejandro Corvalán
Contribuciones
L.G., A.M., W.A., A.C. y L.P. redactaron el manuscrito principal; M.J.M., P.C. y M.E.T. realizaron la MTS. y LDH. ensayo: K.V. y G.A. realizaron el ensayo TUNEL, de caspasas y de muerte. L.P. preparó la Fig. 1; L.G., K.V. y G.A. prepararon las Figs. 2, 3, 4, 5, 6 y 7; W.A. realizó el análisis de acoplamiento, Fig. 8 y Tabla 2. G.B. y A.C. contribuyeron a la revisión del manuscrito. Todos los autores revisaron la versión final del manuscrito.




